Wizard Magne Sil 基因组 DNA 纯化系统是使用一种固相顺磁性硅质顆粒来纯化基因组 DNA。该技术取代了以真空过滤和离心为基础的 DNA 纯化形式,而且还使样本处理更加经济、高效。
试剂、试剂盒
全血口腔涂片或样品污染物二硫苏糖酵乙醇异丙醇裂解缓冲液
仪器、耗材
自动定位器P250 盒装吸头 血液基因组高产量系96 孔收集板BiomekFX 自动机械工作平台分离装置传热板储液器微量吸头离心架筐加热块磁分离架DNAIQ系统
实验步骤
方法1:利用液体处理自动机械工作平台从20ul全血中进行基因组DNA的高产率分离
这个方法用于对在液体处理自动机械,如BiomekFX和Biomek2000实验自动工作平台(BeckmanCoulter)上安装的96孔板内的20ul血液样品进行处理。如果用单头的设备对单个板进行处理,所需的时间还不到lh。
将血液与去垢剂-促溶剂、裂解/结合缓冲液混合,既可以破坏细胞及其核膜,又可以使
蛋白质变性。释放出的DNA被吸附在裂解/结合缓冲液中的MagneSil顆粒表面,而粘有靶复合体的磁珠被外部磁场捕获到样品板孔的側面,随后裂解液作为废液而被去除。残留的污染物经下面的一系列洗涤过程被去除:首先用裂解/结合缓冲液,然后用盐洗涤液,最后用乙酵/盐洗涤液以除去最后残留的微董亚铁血红素。磁珠干燥后,在一个传热板上用TE缓冲液或水来洗脱DNA。
一、材料
1.特殊的设备
3台单位置的实验用自动定位器(BeckmanCoulter)
4套P250盒装吸头(BeckmanCoulter)
4X4位置实验用自动定位器(BeckmanCoulter)
96孔收集板(Promega,A9161或类似产品)
96孔吸头洗涤自动实验用定位器(BeckmanCoulter)
装有单舱和一个96孔移液器头的BiomekFX自动机械工作平台(BeckmanCoulter)
深孔MagnaBot96孔磁性分离装置(Promega)
深孔多孔板(Marsh,AB-0932[2.2ml]和AB-0787[1.2ml]或类似产品)
传热板(Promega,Z3271或类似产品).
加热和冷却自动实验用定位器(BeckmanCoulter)
MagnaBot边条,l/8in(lin=2.54cm)(Promega)
回旋振荡式自动实验用定位器(BeckmanCoulter)
底部为锥形的96孔储液器(InnovativeMicroplates,S30014或类似产品)
吸头装卸自动实验用定位器(BeckmanCoulter)
2.其他
MagneSil血液基因组高产董系统(Promega;该系统包括乙酵洗海液、抗泡沫试剂、裂
解缓冲液、盐洗涤液、洗脱缓冲液和MagneSil顺磁性顆粒)
3.细胞和组织
全血、口腔涂片或样品污染物
二、方法
1.将400ul裂解缓冲液和40ulMagneSil顆粒加到200ul血样中,利用剧烈的机械混合裂解白细胞,并使释放出的DNA与磁性颗粒(PMP)结合。
2.用MagnaBot磁场捕获颗粒,弃去液体。
3.用360ul裂解缓冲液彻底洗涤PMP。
4.用MagnaBot磁场捕获顆粒,弃去液体。
5.用360ul盐缓冲液彻底洗涤PMP。
6.用MagnaBot磁场捕获顆粒,弃去液体。
7.重复步骤5和6,使盐洗涤的总次数达到2次。
8.用360ul乙醇洗涤缓冲液彻底洗涤PMP。
9.用MagnaBot磁场捕获顆粒,弃去液体。
10.重复步骤8和9,使乙酵洗涤缓冲液洗涤的总次数达到3次。
11.在一个加热块上干燥PMP以除去所有残留的乙醇洗涤缓冲液。
12.在80°C加热块上与210ul洗脱缓冲液剧烈混合以洗脱DNA。孔内温度约为65°C。
13.将洗脱出的DNA储存于-20°C。
方法2:从污染物和口腔涂片中分离基因组DNA的DNAIQ分离法
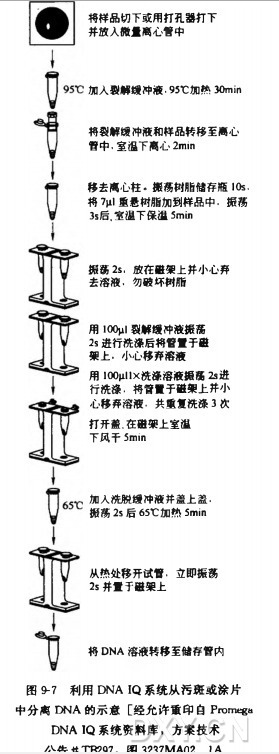
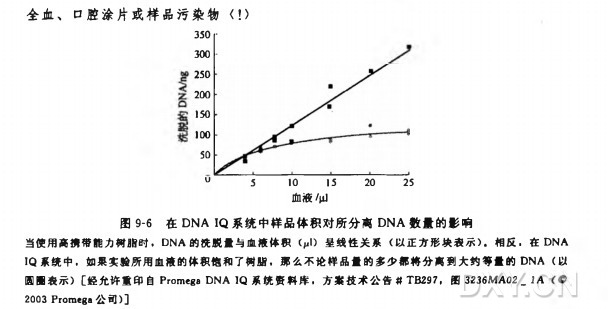
DNAIQ分离系统利用了一种崭新 的DNA分离方法。利用MagneSil化学可以对多种样品中一定量的DNA进行捕获和释放。颗粒有一定携带DNA的能力,若DNA过多则只能结合一定董 的核酸(图9-6)。因此,通常此方法用于分离约l00ngDNA的实验,而不必考虑样品量的大小。用 100ul 洗脱缓冲液洗脱 DNA 使其终浓度达到 lng/ul。结果由该方法分离到的 DNA 不需要进行纯化后的定量。图 9-7 给出了这个方案的流程。
一、材料
1.缓冲液、溶液和试剂
二硫苏糖酵(DTT),lmol/L
乙醇,95%?100%
异丙醇
裂解缓冲液
确定使用裂解缓冲液的总量(表9-3)。毎100ul裂解缓冲液(随DNAIQ系统一起提供)中加入1ul 1moL/L的DTT,颠倒数次使其混合,标记已加有DTT并注明日期。裂解缓冲液在室溫下储存不得超过1个月。

2. 特殊设备
抗气溶胶的微量吸头
DNAIQ 离心架筐(Promega,V1221)
加热块
MagneSphere 技术磁分离架(Promega)
微量离心管,1.5 ml 圆锥形(Promega,V1231)
3. 其他
DNAIQ 系统(Promega; 该系统包括树脂、裂解缓冲液、2X 洗涤缓冲液和洗脱缓冲液)
微量离心管,1.5 ml(Promega,V1231)
二、方法
1. 将样品(见表 9-3) 置于 1.5 ml 微量离心管中。切记:推荐用量的树脂可捕获 DNA 的最大量约为 l00ng。
2. 加适量备好的裂解缓冲液,不同样品需用不同体积的裂解缓冲液,参见表 9-3 的第 2栏(裂解缓冲液 1) 以确定适合的用量。盖上管盖,将试管置于 95°C 加热块上放 30 min。对于小污斑,替代方法是将受污染材料置于一个装有 1.5 ml 微量离心管的 DNAIQ 离心柱内,并向柱内加入 100?150ul 裂解缓冲液。小心盖上管盖,95°C 加热 30 min#如果使用图 9-7 中所示的微量离心管和离心柱,那么绝大部分的缓冲液将会留在离心管内,继续进行第 4 步。若样品所需裂解缓冲液的体积超过150ul, 不宜使用该方法。
3. 从加热块上移去试管,将裂解缓冲液和样品转移到 1.5 ml 微量圆锥形离心管内的离心柱中。为得到最大量的污染物应将裂解缓冲液与受污染的基质一起离心,这一点很重要。
4. 在室温下以最大转速离心 2 min, 移去离心柱。
5. 高速涡旋振荡树脂储存瓶 l0s 使其彻底混合,将 7ul 树脂加到 DNA 溶液中,加树脂时要保持重悬状态以获得相同的结果。
6. 高速涡旋振荡样品/裂解缓冲液/树脂混合物 3s,室温下保温 5 min。
7. 高速涡旋振荡试管 2s, 将其置于磁架上将会立刻出现分离现象。
8. 小心移弃所有溶液,切勿破坏管侧面上的树脂。
9. 加入 100ul 裂解缓冲液,从磁架上移开试管,高速涡旋振荡 2s。
10. 将试管重新放置到磁架上,移弃全部裂解缓冲液。
11. 加入 100ul1X 洗涤缓冲液,从磁架上移开试管,高速涡旋振荡 2s。
12. 将试管重新放置到磁架上,移弃全部洗涤缓冲液。
13. 重复步骤 11 和 12 两次,以使总洗涤次数达到 3 次,最后一次洗涤后要移弃所有溶液。
14. 打开试管盖,在磁架上风干树脂 5 min。
15. 加入 l00ul 洗脱缓冲液。
16. 盖上管盖,高速涡旋振荡试管 2s, 将试管置于 65°C 5 min。
17. 从加热块上移开试管,高速涡旋振荡 2s 后,立即将试管置于磁架上。
18. 将溶液转移到新容器内,DNA 的浓度约为 1ng/ul,可以直接用于扩增反应。DNA 溶液可在 4°C短期储存,或在-20°C 或-70°C 长期储存。
此文转载来源:丁香通

